
初中化学“导学案”高效教学模式
泸县宋贵清工作室 朱斌
一、导学案要解决的主要问题
化学备课组的导学案要求反映出我校提出的“三环五步”教学模式。
“三环”包括“预习”、“探究”、“练习”,“五步”是指课堂三环节的具体实现过程,包括“学”、“展”、“点”、“练”、“结”等学生在课堂中的学习过程。
学:学生自主学习,包括课前预习、课内自学等
展:学生自主学习成果展现,包括了小组讨论、师生互动、学生实践(实验)活动呈现等。
点:教师适当点拨,解决知识难点、强调重点
练:学生练习巩固
结:学生对当堂课的学习活动进行小结
二、导学案的主要内容
1、学生对每节课学习的内容要有明确的目标。
学生自主学习要有方向,每节课该学习哪些知识点,该弄明白哪些问题,心中都应该有个谱。因此,导学案第一步就是明确学习目标,让学生沿着目标进行学习。学习目标要让学生清楚他们每次探究的问题目的是什么?会涉及到哪些重要知识?避免学生学习的盲目性,提高学习的效率。传统的教学模式是教师一进教室就讲课,虽然在强调每一个知识点,但只是让学生被动接受知识。该过程往往是学生先学知识,再明目标,这使学生失去了主动学习的欲望。
2、强调学生养成课前预习的习惯
课前预习是培养学生养成终生学习习惯的好方法,但这也是教师执行导学案的一个难点所在。去年我校的导学案都有预习问题展示这一步,刚开始还能让学生完成预习过程,但随着学生课业负担加重,大多数学生放弃了这一步。通过备课组讨论总结,预习提问应该是小组合作交流所要解决的问题,所以,预习应该是让学生提前为课堂上的合作探究作好充分的准备。学生先独立思考,试着完成课堂上要探究的课题、要交流的内容,自己明白的地方准备交流展示,不明白的地方作好记号,课堂上与组员进行讨论。如“探究空气组成成分”的活动,学生在课前先独立完成探究过程,对提出的问题作出假设,先设计好实验,预做一下实验,以便课堂展示,准备好实验仪器带到课堂上演示,针对不理解的地方准备好要讨论的问题等。因此,学生的预习应该是学生先独立思考的,准备课堂上交流和解惑的过程。
3、“教学案-学案”编写要基本一致
(1)、学案备课总的要求是:提前集体备课、以备课小组为单位进行集体备课,研究课标和教材,分析学生学习状态,在此基础上确定学案的编写策略,确定每个教师编写的任务。轮流主备(至少两人教同年级同学科者)、集体研讨、撰写学案、师生共用。在每个单元或章节教学之前,上课前两天将“学案”发给学生,任课教师对“学案”再次进行阅读理解和补充。第二天师生共用“学案”实施课堂教学,课后教师在“教学案”的有关栏目或空白处填写“课后记”,用于下次集中研讨备课的交流。这是一个不断打磨、不断提升的过程,经验得以积累,教训和问题便成了复习教学的重点和难点。学生则在“学案”相关栏目或空白处填写学习心得等。
(2)、“学案”首先要具备明确的学习目标,第二应注意帮助学生梳理知识结构体系,第三提供适当的学习方法和学习策略的指导,第四提供检测学习效果的适当材料,第五注意“学案”备课与一般教案和讲义的区别,不能把“学案”写成类似学习辅导用书的模式‘第六不同学科、不同类型的“学案”都应该有各自不同的角色。总体上说,“学案”的编写主要按授课进行,与教师上课同步,适合于不同课型的教学需要。
(3)、学案编写主要按课时进行,每课时一案。
4、学案结构确定哪些内容
(1)、学习目标 (2)、预习导学 (3)、问题探究 (4)、检测反馈 (5)、拓展延伸 (6)、学后记
5、学案编写应遵循的原则
(1)、导学性原则:具有指导学生自学的功能。
(2)、探究性原则:尽可能设计可供学生探究的问题。
(3)、层次性原则:关照到不同学力学生的学习需求。
(4)、创新性原则:有利于培养学生创新意识。
6、应针对学生的使用的要求:
①根据“学案”内容认真进行课本预习。所有同学必须自行解决“学案”中的基础部分。学有余力的同学可以做提高题,碰到生疏的、难以解决的问题要做好标记,第二天与同学交流或在课堂上向老师质疑。要求学生在使用“学案”时坚持三原则:自觉性原则、主动性原则、独立性原则。
②课堂上注意作学习方法和规律的笔记以便今后复习,学完一课后,要在“学案”的空白处写上“学后记”(学习心得)。
③每隔一定时间后,将该科“学案”进行归类整理,装订成复习资料(一般以月为单位),注意保存。
7、针对教师如何使用“学案”
①原则上不允许再布置课外作业,应该指导学生使用“学案”,在上课前必须抽批部分“学案”,以了解学情,收集错例,认真反思,再次进行课前备课,针对学案要进行面批、个别辅导,必须做到“日清”、“周清”。
②用“学案”进行课堂教学时,要努力做到:新知识让学生主动探索;课本放手让学生阅读;重点和疑点放手让学生讨论;提出的问题放手让学生思考解答;结论或中心思想等放手让学生概括;规律放手让学生寻找;知识结构体系放手让学生构建。
③用“学案”进行课堂教学时,要拓展学生的思维,主要包括:第一引导学生通过展开充分的思维来获得知识,暴露学生思维过程中的困难、障碍、疑问和错误;第二寻找学生思维的闪光点及时给予鼓励和引导;第三课堂教学中除充分调动学生的思维外,教师自己的思维也要充分展开,在教学过程中激活学生,提升自己,做到教学相长。
④“学案”中巩固训练题的设计至少分四类:A类(一般学生实践)、B类(中等水平学生实践)、C类(学有余力学生)、D类(拓展题)。要求各学科教师必须大量查阅资料、认真搜集设计各种类型的训练题目,以满足各类学生的需求。
⑤用“学案”进行教学要做到“四精四必”:精选、精讲、精练、精批,有发必收,有收必批,有批必评,有评必补。在课堂教学的实施过程中,教师好比导演,要为学生创造表演的舞台,让课堂充满魅力。教师必须根据教材内容,灵活使用教学手段,做到寓教于乐,寓教于趣,寓教于情,使学生处于学习的亢奋状态。
⑥要求各学科教师在学校统一举行的抽测中,试卷题目必须是当月“学案”中的训练题目的再次精选。
三、导学案的价值意义及创新点
捷克著名的教育家夸美纽斯说过这样一句话:“找出一种教育方法,使教师因此可以少教,但是学生多学。”
新课标要求:教师是学生学习的促进者,帮助学生决定适当的学习目标,并寻找达到目标的最佳途径;指导学生形成良好的学习习惯,掌握学习策略,发展学生的基本认识能力,提高学生的学力水平;创设丰富的教学情景,信任学生的学习能力,激发学生的学习动机,培养其学习兴趣,充分调动学生的学习积极性,营造一个轻松宽容的课堂氛围;为学生提供各种便利,为学生服务;建立一个接纳的、支持的、宽容的学习氛围,给学生以心理上的支持;作为学习的参与者,与学生分享自己的感情和想法;和学生一道寻找真理,能够承认自己的失误;对学生的评价,不再是分等级的“筛子”,而是激发前进的“泵”;不把知识作为“绝对的客观真理”强加给学生,把学生学习知识的过程真正当作是一个主动建构的过程。教师由学生学习的指导者变为学生学习的策划者、组织者、促进者、引导者,从而在根本上改变了学生的学习方式。
本课题的研究就是以以上的理论和要求为基准,力图尽快变革课堂教学中与以上理论和要求相悖的理念和行为,如果本课题的研究取得成功,精心设计和编写出符合要求的《导学案》,这将为学生的自主学习提供六个作用:①学生自主学习的路线图,为学生高效地自主学习提供有效途径;②课堂知识结构体系的呈现表;③学生课堂展示的备份材料;④学生课堂学习的随堂记录本;⑤自我反思小结的文本材料;⑥以后复习巩固使用的学习材料。当然《导学案》设计质量的高低决定了学生的学习质量,让学生能够通过教师设计的导学案增长知识、形成能力。
通过“学案导学”这一教学策略,解决“以学生为中心”的主体参与、自主学习为主体地位的问题,变“被动学习”为主动学习。实现两个前置:即学习前置和问题前置。使学生能够在学案的引导之下,通过课前自学、课堂提高、课后链接等环节的调控,降低学习难度。而教师则借助“学案导学”这一策略,能够将教材有机整合,精心设计,合理调控课堂教学中“教”与“学”,从而极大的提高课堂教学效率。学生通过自主、合作、探究、交流、展示、反馈,等学习活动,使学生真正成为学习的主人。
读《思维可视化教学》体会
朱斌
工作室分发了一本《思维可视化教学》,偶尔看看,受益匪浅。现将体会叙述如下。
1、可视化的魅力
《思维可视化教学》这本书让我深深感受到了可视化的魅力。可视化不仅仅是将信息转化为图像,更是一种艺术,一种将复杂信息以简单明了的方式表达出来的艺术。读完这本书,我明白了可视化在教学过程中的重要性。它不仅有助于学生更好地理解和记忆知识,还可以激发他们的学习兴趣和想象力。
2、思维构建的重要性
这本书还让我认识到了思维构建的重要性。通过可视化教学,我们可以帮助学生更好地构建知识框架,培养他们的逻辑思维能力。通过清晰的图像和简洁的文字,学生可以更快地抓住知识的核心,深入理解概念。同时,可视化教学还有助于培养学生的创新思维和问题解决能力,让他们在未来的学习和生活中更加游刃有余。
3、对未来的展望
阅读《思维可视化教学》,让我对未来教育充满了期待。我相信,随着可视化技术的不断发展,未来的教育将更加注重学生的思维训练和全面发展。可视化将成为教学的重要组成部分,学生将更加主动地参与到学习过程中,探索未知的世界。
总结:
《思维可视化教学》这本书让我深刻认识到了可视化在教学中的潜力和价值。通过将复杂信息转化为简单的图像,可视化不仅可以帮助学生更好地理解和记忆知识,还可以激发他们的学习兴趣和想象力。同时,可视化教学还有助于培养学生的逻辑思维能力、创新思维和问题解决能力,让他们在未来的学习和生活中更加出色。我相信,未来的教育将更加注重学生的思维训练和全面发展,可视化将成为教学的重要组成部分。
7.1第七单元 常见的酸和碱
总编号:NO. 第一节 第1课时 常见的酸
活 动 探 究
1、写出你所知道的酸,并进行分类,总结规律,你能得出什么结论?
强酸:硫酸 盐酸 硝酸 弱酸:碳酸_______ 中强酸:醋酸_______ 酸溶于水后解离出的阳离子全部是___________。
2、观察实验和盐酸、硫酸的标签完成。
物性 | 颜色 | 状态 | 气味 | 密度 | 质量分数 | 敞开现象 | 其他 |
浓盐酸 |
|
|
|
|
|
|
|
浓硫酸 |
|
|
|
|
|
|
|
3闻气味的方法:应使容器口远离鼻孔,用手轻轻________,让少量的气体飘进鼻孔。
4、浓盐酸具有较强的_______性,是_________气体溶于水形成的溶液,又叫氢氯酸,打开瓶盖会看到瓶口有_________出现,原因是____________________________________________________________。
5、浓硫酸有较强的________性,因而常用作气体___________剂;浓硫酸有 “________” 性,沾在皮肤或衣物上会出现 碳化 现象;浓硫酸有强烈的_________性,因而使用时要特别小心,如果浓硫酸不慎沾到皮肤上,应立即用大量的____冲洗,然后涂上3%~5%的___________溶液,以防灼伤皮肤;浓硫酸溶于水会释放______________,因此在稀释时,应将__________倒入_________中,并且不断搅拌。
拓 展 练 习
A.单质 B.化合物 C.纯净物 D.混合物
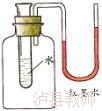
2、红墨水液面上升,左边支管的红墨水液面降低,则加入的物质不可能是 ( )
A.氢氧化钠 B.生石灰 C.硝酸铵 D.浓硫酸
3、如果将浓硫酸和浓盐酸敞口放置一段时间后,溶液质量、溶质质量、溶剂质量会发生怎样的变化?
| 溶质质量 | 溶剂质量 | 溶液质量 | 溶质质量分数 |
浓盐酸 |
|
|
|
|
浓硫酸 |
|
|
|
|
由上分析可知:浓盐酸和浓硫酸都要__________保存。
4、酸的分类与命名中,①根据酸中是否含氧元素分为含氧酸和无氧酸,含氧酸读作“某酸”如:H2SO4读作“硫酸”,则H3PO4读作:“___________”,无氧酸读作“氢某酸”,如HCl可读作“氢氯酸”,则H2S读作“___________”,HF可读作“___________”。②根据从酸分子中可以电离出H+的个数分为一元酸(如HCl)、二元酸(如H2SO4)、三元酸(如H3PO4)。判断CH3COOH属于______元酸。
5、下列关于浓硫酸的描述错误的是
A.溶于水时放出大量的热 B.有强烈的腐蚀性
C.稀释浓硫酸时,切不可将水倒进浓硫酸中 D.可在量筒中用浓硫酸配制稀硫酸
6、将浓硫酸、浓盐酸敞口放置一段时间,它们的共同变化是 ( )
A.颜色发生改变 B.发生化学变化 C.质量减少 D.溶质的质量分数变小
7、已知溴化物中溴元素(Br)显-1价,则溴化氢的化学式为____________ ,它溶于水形成的酸的名称叫____________酸 。已知硒元素(Se)的某化合物H2SeO4,则该物质的化学名称叫__________ ,其中硒元素的化合价为__________。
鲁教版九年级下册《第7单元 常见的酸和碱》单元测试卷
可能用到的相对原子质量:
一、我会选(每题3分,共24分)
1.向2mL氨水中滴加5~6滴紫色石蕊试液,充分振荡后溶液颜色将变成( )
A.红色B.紫色 C.无色 D.蓝色
2.如表列出了一些常见物质在常温下的pH范围,其中呈碱性的是( )
物质名称 | 鸡蛋清 | 牛奶 | 西红柿 | 柠檬汁 |
pH范围 | 7.6~8.0 | 6.3~6.6 | 4.0~4.4 | 2.0~3.0 |
A.鸡蛋清B.牛奶 C.西红柿 D.柠檬汁
3.化学实验室通常将药品分类后存放在不同的药品柜内,现存放的部分药品如下表所示:
药品柜 | 甲 | 乙 | 丙 | 丁 |
药品 | 盐酸、硫酸 | 氢氧化钠、氢氧化钙 | 氯化钠、硫酸钠 | 铁、铝 |
实验室新购进一些硫酸铜,你认为它应存放在药品柜( )
A.甲B.乙 C.丙 D.丁
4.某同学在实验室测定了几种溶液的pH,其结果如下表:
溶液 | 盐酸 | CuCl2溶液 | Na2SO4溶液 | 水 | Na2CO3溶液 | NaOH溶液 |
pH | <7 | <7 | =7 | =7 | >7 | >7 |
该同学由此得出的结论正确的是( )
A.盐溶液可能显酸性、碱性或中性 B.pH>7一定是碱溶液
C.pH=7一定是盐溶液 D.pH<7一定是酸溶液
5.某城市水质硬度较大,容易产生水垢(细小的碳酸钙颗粒),长期使用的毛巾很容易变滑腻,你觉得可以选用厨房中的哪一种物品将水垢除去( )
A.食盐B.花生油 C.蔗糖 D.食醋
A.用盐酸除铁锈 B.服用含有氢氧化镁的药物治疗胃酸过多
C.用熟石灰改良酸性土壤 D.用硫酸处理印染厂含碱废水
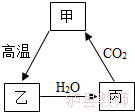
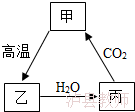
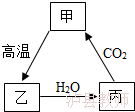
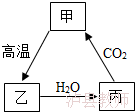
7.根据如图甲、乙、丙三种物质的转化关系,推测丙可能为( )
A.碳酸钙 B.氧化钙 C.氢氧化钙 D.碳酸钠
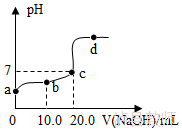
A.b、d点对应溶液的pH:b>d
B.所用氢氧化钠溶液的质量分数一定为30%
C.向b点对应的溶液中滴加石蕊溶液,溶液呈无色
D.d点对应的溶液中溶质是NaCl和NaOH
二、我会填(共25分)
9.(3分)如图所示,电子秤上的量筒中分别盛有蒸馏水、浓硫酸,放置一段时间。
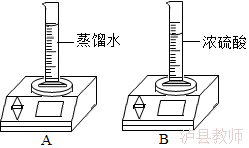
(2)B中示数 (填“变大”“不变”或“变小”),其原因是 。
10.(3分)分析下列反应,回答有关问题.
①2KOH+CO2═K2CO3+H2O ②2NaOH+CO2═Na2CO3+H2O
③Ca(OH)2+CO2═CaCO3↓+H2O
(1)由上述反应可知,碱与二氧化碳反应的规律是都生成 和水;
(2)根据上述规律,写出Ba(OH)2与CO2反应的化学方程式 ;
(3)用CO2鉴别NaOH和Ca(OH)2两种溶液时,能观察到明显现象的是 溶液.
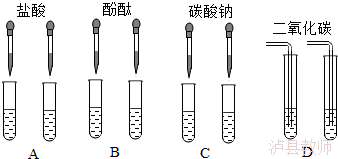
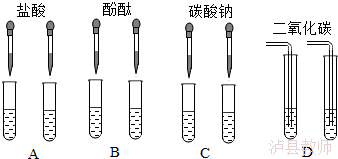
11.(4分)甲同学为了区别氢氧化钠和氢氧化钙溶液,设计了如下图所示的四组实验方案.
(1)其中能达到实验目的的是__________________________________。
(2)在C组实验中发生反应的化学方程式为 。
(3)实验结束后,甲同学将A、C组四支试管中的溶液倒入同一容器中,看到溶液变浑浊,该现象说明有______________(填化学式)生成,滴入酚酞后溶液呈红色.
(4)滴入酚酞后溶液呈红色,说明溶液呈碱性.使溶液呈碱性的物质是什么呢?甲同学进一步推测:溶液中呈碱性的物质可能是碳酸钠、氢氧化钙和_____________三种物质中的一种,或是三种物质两两混合组成的混合物.
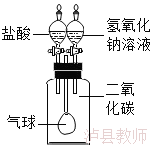
(1)有时药品滴加顺序会影响实验现象。如果观察到的现象是“气球先膨胀,后变瘪”,则加入试剂的顺序应该是 (填序号)
A.先加入盐酸,再加入氢氧化钠溶液 B.先加入氢氧化钠溶液,再加入盐酸
(2)请解释气球“先膨胀”的原因: 。
(3)写出气球“后变瘪”的化学方程式 。
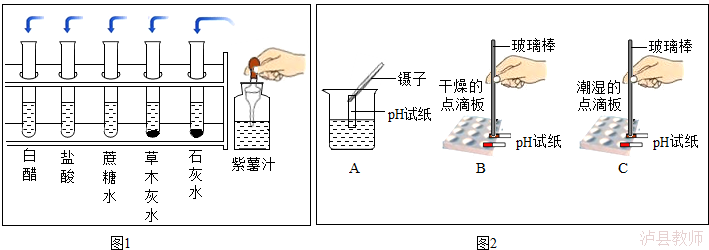
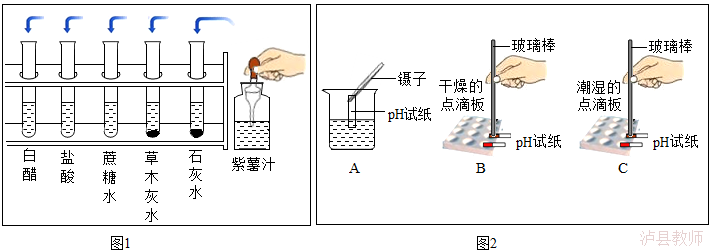
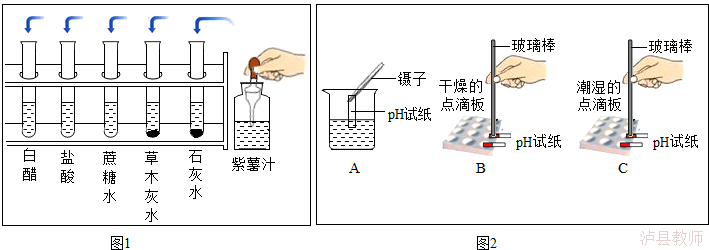
13.(6分)某校同学开展了如下“溶液酸碱性的检验”的实验活动:
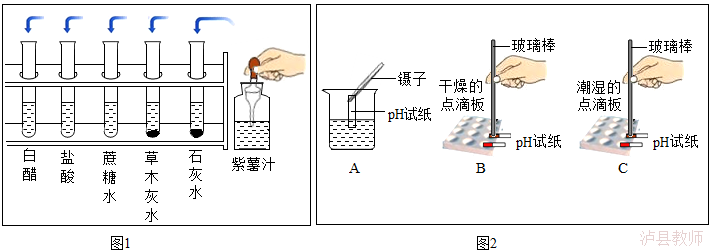
(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如下表所示:
溶液 | 白醋 | 盐酸 | 蔗糖水 | 草木灰水 | 石灰水 |
加入紫薯汁后的颜色 | 红色 | 红色 | 紫色 | 绿色 | 绿色 |
①图1中存放紫薯汁的仪器名称是 ;
②据上表推测,紫薯汁能做酸碱指示剂,遇到稀硫酸溶液可能显示的颜色是 ;
(2)用pH试纸测定图1中部分溶液的酸碱度:草木灰水的pH>7,属于 (填“酸性”“中性”或“碱性”)溶液,白醋的pH (填“>”“<”或“=”)7;
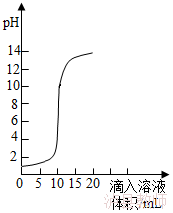
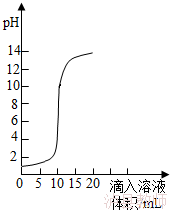
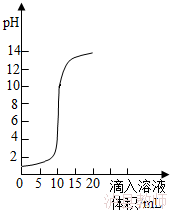
10.(6分)如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线。
(1)氢氧化钠和盐酸恰好完全反应时,溶液的pH 7(填“大于”或“小于”或“等于”)。
(2)根据曲线判断,该反应是将 (填“氢氧化钠溶液”或“盐酸”,下同)滴入 中,理由是 。
(3)当滴入溶液的体积为5mL时,所得溶液中的溶质为 (写化学式),若在此溶液中滴入石蕊试液,溶液显 色。
三、我会探究(13分)
11.(8分)某化学兴趣小组的同学在做氢氧化钙与盐酸中和反应的实验时,忘记滴加指示剂,因而无法判断酸碱是否恰好完全反应.于是他们对反应后溶液中的溶质大胆提出猜想,进行了以下探究,请你和他们一起完成下列实验报告.
【提出问题】该溶液中的溶质含有哪些成分?
【查阅资料】CaCl2溶液呈中性.
【猜想与假设】猜想Ⅰ:溶液中的溶质只有 ;
猜想Ⅱ:溶液中的溶质有CaCl2、HCl;
猜想Ⅲ:溶液中的溶质有CaCl2、Ca(OH)2;
猜想Ⅳ:溶液中的溶质有CaCl2、Ca(OH)2、HCl.
请写出该反应的化学方程式 .经过讨论,同学们直接得出猜想 是不正确的.为了验证余下的哪一种猜想是正确的,同学们又做了以下实验.
【进行实验】
实验操作 | 实验现象 | 实验结论 |
①取少量反应后的溶液于试管中,滴加酚酞溶液 | _________________ | 猜想Ⅲ不正确 |
②再另取少量反应后的溶液于另一支试管中,向里面加入适量碳酸钙 | 有气泡产生 | 猜想 不正确; 猜想 正确 |
有气泡生成的化学方程式为 .
【拓展】还可以单独用下列哪种物质来证明上述猜想是正确的 .
A.CuO B.AgNO3 C.NaOH
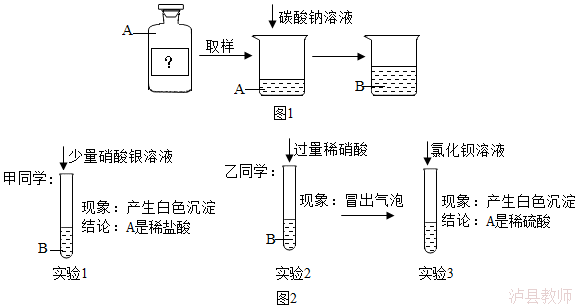
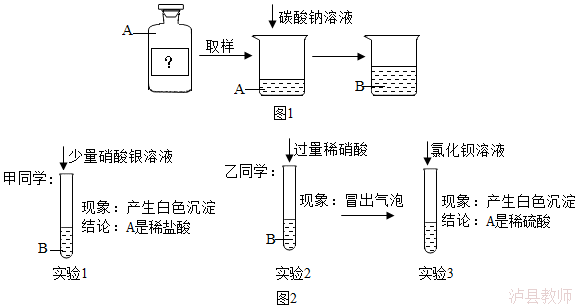
12.(5分)在化学课上,老师带来一瓶未知溶液A,已知它是稀盐酸或稀硫酸中的一种。进行如图1实验:
观察到烧杯中的现象是 。
【提出问题】A是哪一种酸?
老师要求甲、乙同学从反应后的溶液B分别展开探究。
【猜想假设】甲同学:A是稀盐酸;乙同学:A是稀硫酸。
【实验探究】图2
【评价交流】甲同学的实验 (填“能”或“不能”)得出正确结论,乙同学的实验 (填“能”或“不能”)得出正确结论。
实验3发生反应的化学方程式为 ;反应后所得溶液中一定含有的离子是 。
四、我会计算(3分)
13.(3分)将适量二氧化碳通入100g氢氧化钠溶液中。恰好完全反应后,得到108.8g碳酸钠溶液请计算:
(1)参加反应的二氧化碳的质量为 g;
(2)氢氧化钠溶液的溶质质量分数。
鲁教版九年级下册《第7单元 常见的酸和碱》2017年单元测试卷(2)
参考答案与试题解析
一、我会选(每题5分,共40分)
1.(5分)向2mL氨水中滴加5~6滴紫色石蕊试液,充分振荡后溶液颜色将变成( )
A.红色B.紫色 C.无色 D.蓝色
【解答】解:紫色石蕊试液遇酸性溶液变红,遇碱性溶液变蓝色,氨水呈碱性,所以向2ml氨水中滴加5~6滴紫色石蕊试液,充分振荡后溶液颜色将变成蓝色。
故选:D。
2.(5分)如表列出了一些常见物质在常温下的pH范围,其中呈碱性的是( )
物质名称 | 鸡蛋清 | 牛奶 | 西红柿 | 柠檬汁 |
pH范围 | 7.6~8.0 | 6.3~6.6 | 4.0~4.4 | 2.0~3.0 |
A.鸡蛋清B.牛奶 C.西红柿 D.柠檬汁
【解答】解:A、鸡蛋清的pH大于7,显碱性。
B、牛奶的pH小于7,显酸性。
C、西红柿的pH小于7,显酸性。
D、柠檬汁的pH小于7,显酸性。
故选:A。
3.(5分)化学实验室通常将药品分类后存放在不同的药品柜内,现存放的部分药品如下表所示:
药品柜 | 甲 | 乙 | 丙 | 丁 |
药品 | 盐酸、硫酸 | 氢氧化钠、氢氧化钙 | 氯化钠、硫酸钠 | 铁、铝 |
实验室新购进一些硫酸铜,你认为它应存放在药品柜( )
A.甲B.乙 C.丙 D.丁
【解答】解:硫酸铜是由铜离子和硫酸根离子组成的化合物,属于盐,氯化钠和硫酸铜属于盐,所以纯碱应该放在丙药品柜中。
故选:C。
4.(5分)某同学在实验室测定了几种溶液的pH,其结果如下表:
溶液 | 盐酸 | CuCl2溶液 | Na2SO4溶液 | 水 | Na2CO3溶液 | NaOH溶液 |
pH | <7 | <7 | =7 | =7 | >7 | >7 |
该同学由此得出的结论正确的是( )
A.盐溶液可能显酸性、碱性或中性
B.pH>7一定是碱溶液
C.pH=7一定是盐溶液
D.pH<7一定是酸溶液
【解答】解:A、CuCl2溶液的pH小于7,显酸性;Na2SO4溶液的pH等于7,显中性;Na2CO3溶液的pH大于7,显碱性,因此盐溶液可能显酸性、碱性或中性,故选项正确。
B、Na2CO3溶液的pH大于7,显碱性,但是碳酸钠溶液是盐溶液,故选项错误。
C、水的pH等于7,显中性,因此pH=7的溶液不一定是盐溶液,故选项错误。
D、CuCl2溶液的pH小于7,显酸性,但CuCl2溶液是盐溶液,不是酸溶液,故选项错误。
故选:A。
5.(5分)某城市水质硬度较大,容易产生水垢(细小的碳酸钙颗粒),长期使用的毛巾很容易变滑腻,你觉得可以选用厨房中的哪一种物品将水垢除去( )
A.食盐B.花生油 C.蔗糖 D.食醋
【解答】解:厨房中能用来除去水垢的物质是食醋,水垢的主要成分是碳酸钙与氢氧化镁,两者均能与醋酸反应生成可溶于水的物质。
故选:D。
6.(5分)中和反应在生活中有广泛应用.下列应用不属于中和反应的是( )
A.用盐酸除铁锈
B.服用含有氢氧化镁的药物治疗胃酸过多
C.用熟石灰改良酸性土壤
D.用硫酸处理印染厂含碱废水
【解答】解:A、用盐酸除铁锈,该反应的反应物是金属氧化物和酸,不是酸与碱生成盐和水的反应,不属于中和反应,故选项正确。
B、服用含有氢氧化镁的药物治疗胃酸过多,氢氧化镁与盐酸反应生成氯化镁和水,该反应是酸与碱反应生成盐和水的反应,属于中和反应,故选项错误。
C、用熟石灰改良酸性土壤,熟石灰与酸反应生成盐和水,该反应是酸与碱反应生成盐和水的反应,属于中和反应,故选项错误。
D、用硫酸处理印染厂含碱废水,该反应是酸与碱反应生成盐和水的反应,属于中和反应,故选项错误。
故选:A。
7.(5分)根据如图甲、乙、丙三种物质的转化关系,推测丙可能为( )
A.碳酸钙B.氧化钙 C.氢氧化钙 D.碳酸钠
【解答】解:碳酸钙在高温的条件下会分解为氧化钙和二氧化碳气体;氧化钙能与水反应生成氢氧化钙;氢氧化钙能与二氧化碳反应生成碳酸钙沉淀和水。
根据图中物质间的转化关系,丙可以与二氧化碳反应生成甲,而甲高温生成乙,乙与水反应生成丙,则推测甲、乙、丙三种物质分别为碳酸钙、氧化钙、氢氧化钙,代入检验。
故选:C。
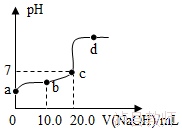
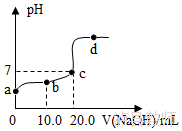
8.(5分)25℃时,向20.0mL质量分数为30%的盐酸中滴加氢氧化钠溶液,溶液的pH与所加氢氧化钠溶液的体积如图所示,下列有关叙述正确的是( )
A.b、d点对应溶液的pH:b>d
B.所用氢氧化钠溶液的质量分数一定为30%
C.向b点对应的溶液中滴加石蕊溶液,溶液呈无色
D.d点对应的溶液中溶质是NaCl和NaOH
【解答】解:A.由图可知,b点所示溶液的pH<7;d点所示溶液的pH>7,所以b、d点对应溶液的pH:b<d,故错误;
B.由化学方程式可知:NaOH+HCl=NaCl+H2O
40 36.5
由于题干中没有提及两种溶液的密度,所以无法确定所需氢氧化钠溶液的溶质质量分数,故错误;
C.由图可知,b点所示溶液的pH<7,溶液显酸性,滴加紫色的石蕊试液变红色,故错误;
D.d点所示溶液的pH>7,所示溶液的溶质既有酸碱中和生成的氯化钠,还有过量的氢氧化钠,故正确。
故选:D。
二、我会填(共32分)
9.(12分)某校同学开展了如下“溶液酸碱性的检验”的实验活动:
(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如下表所示:
溶液 | 白醋 | 盐酸 | 蔗糖水 | 草木灰水 | 石灰水 |
加入紫薯汁 后的颜色 | 红色 | 红色 | 紫色 | 绿色 | 绿色 |
①图1中存放紫薯汁的仪器名称是 滴瓶 ;
②据上表推测,紫薯汁能做酸碱指示剂,遇到稀硫酸溶液可能显示的颜色是 红色 ;
(2)用pH试纸测定图1中部分溶液的酸碱度:草木灰水的pH>7,属于 碱性 (填“酸性”“中性”或“碱性”)溶液,白醋的pH < (填“>”“<”或“=”)7;
(3)图2是三位同学分别测定土壤酸碱度的操作示意图,其中正确的是 B (填“A”“B”或“C”,下同),可能导致被测溶液pH数值发生改变的错误操作是 C 。
【解答】解:(1)①根据实验室常用仪器可知:存放紫薯汁的仪器名称是滴瓶;
②上表推测,紫薯汁遇到稀硫酸溶液可能显示的颜色是红色,紫薯汁在酸碱溶液中显示不同颜色,可以作为酸碱指示剂;
(2)用pH试纸测定图1中部分溶液的酸碱度:草木灰水pH>7,属于碱性溶液;白醋pH<7;
(3)正确的pH试纸的使用方法是取待测液少许涂与其上进行检验,故答案为:C把pH试纸润湿会使溶液被稀释导致数值不准确,A直接放入待测液中会使溶液被污染。
故答案为:
(1)①滴瓶;②红色;
(2)碱性;<;
(3)B;C。
10.(12分)如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线。
(1)氢氧化钠和盐酸恰好完全反应时,溶液的pH 等于 7(填“大于”或“小于”或“等于”)。
(2)根据曲线判断,该反应是将 氢氧化钠溶液 (填“氢氧化钠溶液”或“盐酸”,下同)滴入 盐酸 中,理由是 在未滴入溶液之前,溶液的pH小于7,酸性溶液 。
(3)当滴入溶液的体积为5mL时,所得溶液中的溶质为 NaCl、HCl (写化学式),若在此溶液中滴入石蕊试液,溶液显 红 色。
【解答】解:(1)氢氧化钠和盐酸恰好完全反应时,氢离子和氢氧根离子均无剩余,溶液显中性,pH=7,故答案为:等于;
(2)根据图象,在反应未进行时,溶液的pH=1,为强酸性溶液,所以该曲线反应是将氢氧化钠溶液滴入盐酸中。故填:氢氧化钠溶液;盐酸;在未滴入溶液之前,溶液的pH小于7,酸性溶液;
(3)盐酸和氢氧化钠的反应原理是:HCl+NaOH=NaCl+H2O,滴入氢氧化钠溶液的体积为5mL时,溶液仍为强酸性,所以是氢氧化钠只和部分盐酸反应,所得溶液中的溶质有生成的氯化钠也有剩余的盐酸,酸使石蕊显红色,故答案为:NaCl、HCl;红。
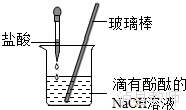
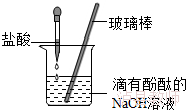
11.(8分)某同学用盐酸与氢氧化钠按照如图的方式进行中和反应实验.
(1)反应的化学方程式为 HCl+NaOH=NaCl+H2O ;
(2)向烧杯中逐滴滴入盐酸至过量,在这个过程中,能够说明盐酸与氢氧化钠发生了化学反应的实验现象是 溶液由红色变为无色 .
(3)以下证明盐酸过量的操作及实验现象的叙述正确的是 BD (填字母代号).
A.滴加石蕊溶液,搅拌后溶液变蓝
B.滴加氢氧化钠溶液,搅拌后溶液颜色不变
C.加入蒸馏水,搅拌后溶液颜色不变
D.加入金属Zn片,产生气泡.
【解答】解:(1)盐酸和氢氧化钠发生反应的方程式为:HCl+NaOH═NaCl+H2O;
(2)氢氧化钠呈碱性,能使无色酚酞试液变红,加入盐酸的过程中要不断搅拌,使盐酸与氢氧化钠充分反应,防止局部酸液过量,酚酞在中性或酸性溶液中都显无色,当红色消失时说明盐酸与氢氧化钠发生了反应;
(3)A、滴加石蕊,溶液变蓝,说明氢氧化钠过量,盐酸不足,故A错误;
B、若恰好完全反应,滴加氢氧化钠溶液,溶液颜色应变红,若不变色则说明盐酸过量,故B正确;
C、加蒸馏水不能起到任何作用,故C错误;
D、加入金属Zn片,锌和盐酸反应产生气泡,则说明盐酸过量,故D正确.
故答案为:(1)HCl+NaOH=NaCl+H2O;(2)溶液由红色变为无色;(3)BD.
三、我会探究(18分)
12.(18分)某化学兴趣小组的同学在做氢氧化钙与盐酸中和反应的实验时,忘记滴加指示剂,因而无法判断酸碱是否恰好完全反应.于是他们对反应后溶液中的溶质大胆提出猜想,进行了以下探究,请你和他们一起完成下列实验报告.
【提出问题】该溶液中的溶质含有哪些成分?
【查阅资料】CaCl2溶液呈中性.
【猜想与假设】猜想Ⅰ:溶液中的溶质只有 CaCl2 ;
猜想Ⅱ:溶液中的溶质有CaCl2、HCl;
猜想Ⅲ:溶液中的溶质有CaCl2、Ca(OH)2;
猜想Ⅳ:溶液中的溶质有CaCl2、Ca(OH)2、HCl.
请写出该反应的化学方程式 2HCl+Ca(OH)2═CaCl2+2H2O .经过讨论,同学们直接得出猜想 Ⅳ 是不正确的.为了验证余下的哪一种猜想是正确的,同学们又做了以下实验.
【进行实验】
实验操作 | 实验现象 | 实验结论 |
①取少量反应后的溶液于试管中,滴加酚酞溶液 | 溶液不变色 | 猜想Ⅲ不正确 |
②再另取少量反应后的溶液于另一支试管中,向里面加入适量碳酸钙 | 有气泡产生 | 猜想 Ⅰ 不正确; 猜想 Ⅱ 正确 |
有气泡生成的化学方程式为 2HCl+CaCO3═CaCl2+H2O+CO2↑ .
【拓展】还可以单独用下列哪种物质来证明上述猜想是正确的 A .
A.CuO B.AgNO3 C.NaOH
反应的化学方程式为 2HCl+CuO═CuCl2+H2O .
【解答】解:【猜想与假设】反应可能是一种物质完全反应,另一种物质有剩余:若氢氧化钙过量,则含有氢氧化钙和氯化钙;若盐酸过量,则含有盐酸和氯化钙;也可能是恰好反应:只有氯化钙;氢氧化钙和盐酸反应生成了氯化钙和水,因此反应的方程式为:Ca(OH)2+2HCl═CaCl2+2H2O;可见氢氧化钙与氯化氢不能共存,所以猜想Ⅳ肯定不正确;
【进行实验】
①因为酚酞遇碱会变红色,而结论是猜想Ⅲ不正确,即不含有氢氧化钙,故观察到的现象是溶液不变红色;
②再另取少量反应后的溶液于另一支试管中,向里面加入适量CaCO3,有气泡产生,则证明剩余溶液中含有HCl,则猜想Ⅱ成立,猜想Ⅰ不成立;
碳酸钙能与稀盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
【拓展】因为烧杯内溶液中的溶质含有HCl显酸性,能用氧化铜来检验,如观察到黑色粉末溶解,溶液变成蓝色,则证明猜想Ⅱ成立;盐酸虽然能够和硝酸银反应产生沉淀,但由于其中的氯化钙也能够和硝酸银产生相同的现象,不能选择;HCl不能和排在氢后面的铜反应;氢氧化钠虽然与HCl反应,但是没有明显现象发生,无法检验;
盐酸与氧化铜反应生成氯化铜和水;反应的化学方程式为:CuO+2HCl=CuCl2+H2O.
故答案为:【猜想与假设】CaCl2;2HCl+Ca(OH)2═CaCl2+2H2O;Ⅳ.
【进行实验】溶液不变色,Ⅰ、Ⅱ;2HCl+CaCO3═CaCl2+H2O+CO2↑.
【拓展】A;2HCl+CuO═CuCl2+H2O.
四、我会计算(10分)
13.(10分)测定抗酸药物有救成分的含量胃酸的主要成分为盐酸,胃酸太多导致胃不舒服时,可以考虑服用抗酸药物来中和胃酸.某抗酸药物的有效成分为氢氧化镁,为测定氢氧化镁的含量,小霞同学取一片该药物(规格为1g)于烧杯中,加入20g溶质质量分数为3.65%的稀盐酸,恰好完全反应(假设药物中其他成分可溶于水,但不与盐酸反应).
(1)通过已知数据能求出的量有 ABCD (填字母编号,符合题意的选项都选).
A.每片药物中氢氧化镁的含量 B.反应中生成氯化镁的质量
C.反应后溶液中氯化镁的质量分数 D.20g稀盐酸中水的质量
(2)计算1g该药物中含氢氧化镁的质量(要求写出计算过程).
【解答】解:(1)A、根据氯化氢的质量结合方程式求解氢氧化镁的质量,氢氧化镁的质量除以每片质量(1g),可得每片药物中氢氧化镁的含量;
B、根据氯化氢的质量结合方程式可以求解氯化镁的质量;
C、根据氯化氢的质量结合方程式可以求解氯化镁的质量,反应后溶液的质量为20g+1g=21g,氯化镁的质量除以21g,可得反应后溶液中氯化镁的质量分数;
D、根据20g溶质质量分数为3.65%的稀盐酸,可求氯化氢的质量20g×3.65%=0.73g,则水的质量为20g﹣0.73g=19.27g.
故选ABCD;
(2)设含有氢氧化镁的质量为x
Mg(OH)2+2HCl=MgCl2十2H2O
58 73
X 20g×3.65%
x﹣=0.58g
答:l g药物中含氢氧化镁0.58 g.
故答案为:(1)ABCD;
(2)0.58g.
声明:试题解析著作权属菁优网所有,未经书面同意,不得复制发布日期:2023/9/21 20:13:01;用户:朱斌;邮箱:15348212927;学号:21219361
鲁教版九年级下册《第7单元 常见的酸和碱》单元测试卷
可能用到的相对原子质量:
一、我会选(每题3分,共24分)
1.向2mL氨水中滴加5~6滴紫色石蕊试液,充分振荡后溶液颜色将变成( )
A.红色B.紫色 C.无色 D.蓝色
2.如表列出了一些常见物质在常温下的pH范围,其中呈碱性的是( )
物质名称 | 鸡蛋清 | 牛奶 | 西红柿 | 柠檬汁 |
pH范围 | 7.6~8.0 | 6.3~6.6 | 4.0~4.4 | 2.0~3.0 |
A.鸡蛋清B.牛奶 C.西红柿 D.柠檬汁
3.化学实验室通常将药品分类后存放在不同的药品柜内,现存放的部分药品如下表所示:
药品柜 | 甲 | 乙 | 丙 | 丁 |
药品 | 盐酸、硫酸 | 氢氧化钠、氢氧化钙 | 氯化钠、硫酸钠 | 铁、铝 |
实验室新购进一些硫酸铜,你认为它应存放在药品柜( )
A.甲B.乙 C.丙 D.丁
4.某同学在实验室测定了几种溶液的pH,其结果如下表:
溶液 | 盐酸 | CuCl2溶液 | Na2SO4溶液 | 水 | Na2CO3溶液 | NaOH溶液 |
pH | <7 | <7 | =7 | =7 | >7 | >7 |
该同学由此得出的结论正确的是( )
A.盐溶液可能显酸性、碱性或中性 B.pH>7一定是碱溶液
C.pH=7一定是盐溶液 D.pH<7一定是酸溶液
5.某城市水质硬度较大,容易产生水垢(细小的碳酸钙颗粒),长期使用的毛巾很容易变滑腻,你觉得可以选用厨房中的哪一种物品将水垢除去( )
A.食盐B.花生油 C.蔗糖 D.食醋
A.用盐酸除铁锈 B.服用含有氢氧化镁的药物治疗胃酸过多
C.用熟石灰改良酸性土壤 D.用硫酸处理印染厂含碱废水
7.根据如图甲、乙、丙三种物质的转化关系,推测丙可能为( )
A.碳酸钙 B.氧化钙 C.氢氧化钙 D.碳酸钠
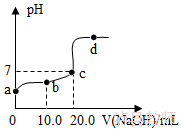
A.b、d点对应溶液的pH:b>d
B.所用氢氧化钠溶液的质量分数一定为30%
C.向b点对应的溶液中滴加石蕊溶液,溶液呈无色
D.d点对应的溶液中溶质是NaCl和NaOH
二、我会填(共25分)
9.(3分)如图所示,电子秤上的量筒中分别盛有蒸馏水、浓硫酸,放置一段时间。
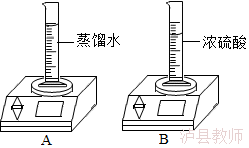
(2)B中示数 (填“变大”“不变”或“变小”),其原因是 。
10.(3分)分析下列反应,回答有关问题.
①2KOH+CO2═K2CO3+H2O ②2NaOH+CO2═Na2CO3+H2O
③Ca(OH)2+CO2═CaCO3↓+H2O
(1)由上述反应可知,碱与二氧化碳反应的规律是都生成 和水;
(2)根据上述规律,写出Ba(OH)2与CO2反应的化学方程式 ;
(3)用CO2鉴别NaOH和Ca(OH)2两种溶液时,能观察到明显现象的是 溶液.
11.(4分)甲同学为了区别氢氧化钠和氢氧化钙溶液,设计了如下图所示的四组实验方案.
(1)其中能达到实验目的的是__________________________________。
(2)在C组实验中发生反应的化学方程式为 。
(3)实验结束后,甲同学将A、C组四支试管中的溶液倒入同一容器中,看到溶液变浑浊,该现象说明有______________(填化学式)生成,滴入酚酞后溶液呈红色.
(4)滴入酚酞后溶液呈红色,说明溶液呈碱性.使溶液呈碱性的物质是什么呢?甲同学进一步推测:溶液中呈碱性的物质可能是碳酸钠、氢氧化钙和_____________三种物质中的一种,或是三种物质两两混合组成的混合物.
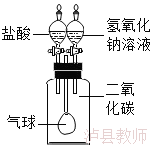
(1)有时药品滴加顺序会影响实验现象。如果观察到的现象是“气球先膨胀,后变瘪”,则加入试剂的顺序应该是 (填序号)
A.先加入盐酸,再加入氢氧化钠溶液 B.先加入氢氧化钠溶液,再加入盐酸
(2)请解释气球“先膨胀”的原因: 。
(3)写出气球“后变瘪”的化学方程式 。
13.(6分)某校同学开展了如下“溶液酸碱性的检验”的实验活动:
(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如下表所示:
溶液 | 白醋 | 盐酸 | 蔗糖水 | 草木灰水 | 石灰水 |
加入紫薯汁后的颜色 | 红色 | 红色 | 紫色 | 绿色 | 绿色 |
①图1中存放紫薯汁的仪器名称是 ;
②据上表推测,紫薯汁能做酸碱指示剂,遇到稀硫酸溶液可能显示的颜色是 ;
(2)用pH试纸测定图1中部分溶液的酸碱度:草木灰水的pH>7,属于 (填“酸性”“中性”或“碱性”)溶液,白醋的pH (填“>”“<”或“=”)7;
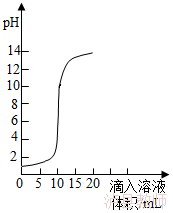
10.(6分)如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线。
(1)氢氧化钠和盐酸恰好完全反应时,溶液的pH 7(填“大于”或“小于”或“等于”)。
(2)根据曲线判断,该反应是将 (填“氢氧化钠溶液”或“盐酸”,下同)滴入 中,理由是 。
(3)当滴入溶液的体积为5mL时,所得溶液中的溶质为 (写化学式),若在此溶液中滴入石蕊试液,溶液显 色。
三、我会探究(13分)
11.(8分)某化学兴趣小组的同学在做氢氧化钙与盐酸中和反应的实验时,忘记滴加指示剂,因而无法判断酸碱是否恰好完全反应.于是他们对反应后溶液中的溶质大胆提出猜想,进行了以下探究,请你和他们一起完成下列实验报告.
【提出问题】该溶液中的溶质含有哪些成分?
【查阅资料】CaCl2溶液呈中性.
【猜想与假设】猜想Ⅰ:溶液中的溶质只有 ;
猜想Ⅱ:溶液中的溶质有CaCl2、HCl;
猜想Ⅲ:溶液中的溶质有CaCl2、Ca(OH)2;
猜想Ⅳ:溶液中的溶质有CaCl2、Ca(OH)2、HCl.
请写出该反应的化学方程式 .经过讨论,同学们直接得出猜想 是不正确的.为了验证余下的哪一种猜想是正确的,同学们又做了以下实验.
【进行实验】
实验操作 | 实验现象 | 实验结论 |
①取少量反应后的溶液于试管中,滴加酚酞溶液 | _________________ | 猜想Ⅲ不正确 |
②再另取少量反应后的溶液于另一支试管中,向里面加入适量碳酸钙 | 有气泡产生 | 猜想 不正确; 猜想 正确 |
有气泡生成的化学方程式为 .
【拓展】还可以单独用下列哪种物质来证明上述猜想是正确的 .
A.CuO B.AgNO3 C.NaOH
12.(5分)在化学课上,老师带来一瓶未知溶液A,已知它是稀盐酸或稀硫酸中的一种。进行如图1实验:
观察到烧杯中的现象是 。
【提出问题】A是哪一种酸?
老师要求甲、乙同学从反应后的溶液B分别展开探究。
【猜想假设】甲同学:A是稀盐酸;乙同学:A是稀硫酸。
【实验探究】图2
【评价交流】甲同学的实验 (填“能”或“不能”)得出正确结论,乙同学的实验 (填“能”或“不能”)得出正确结论。
实验3发生反应的化学方程式为 ;反应后所得溶液中一定含有的离子是 。
四、我会计算(3分)
13.(3分)将适量二氧化碳通入100g氢氧化钠溶液中。恰好完全反应后,得到108.8g碳酸钠溶液请计算:
(1)参加反应的二氧化碳的质量为 g;
(2)氢氧化钠溶液的溶质质量分数。
鲁教版九年级下册《第7单元 常见的酸和碱》2017年单元测试卷(2)
参考答案与试题解析
一、我会选(每题5分,共40分)
1.(5分)向2mL氨水中滴加5~6滴紫色石蕊试液,充分振荡后溶液颜色将变成( )
A.红色B.紫色 C.无色 D.蓝色
【解答】解:紫色石蕊试液遇酸性溶液变红,遇碱性溶液变蓝色,氨水呈碱性,所以向2ml氨水中滴加5~6滴紫色石蕊试液,充分振荡后溶液颜色将变成蓝色。
故选:D。
2.(5分)如表列出了一些常见物质在常温下的pH范围,其中呈碱性的是( )
物质名称 | 鸡蛋清 | 牛奶 | 西红柿 | 柠檬汁 |
pH范围 | 7.6~8.0 | 6.3~6.6 | 4.0~4.4 | 2.0~3.0 |
A.鸡蛋清B.牛奶 C.西红柿 D.柠檬汁
【解答】解:A、鸡蛋清的pH大于7,显碱性。
B、牛奶的pH小于7,显酸性。
C、西红柿的pH小于7,显酸性。
D、柠檬汁的pH小于7,显酸性。
故选:A。
3.(5分)化学实验室通常将药品分类后存放在不同的药品柜内,现存放的部分药品如下表所示:
药品柜 | 甲 | 乙 | 丙 | 丁 |
药品 | 盐酸、硫酸 | 氢氧化钠、氢氧化钙 | 氯化钠、硫酸钠 | 铁、铝 |
实验室新购进一些硫酸铜,你认为它应存放在药品柜( )
A.甲B.乙 C.丙 D.丁
【解答】解:硫酸铜是由铜离子和硫酸根离子组成的化合物,属于盐,氯化钠和硫酸铜属于盐,所以纯碱应该放在丙药品柜中。
故选:C。
4.(5分)某同学在实验室测定了几种溶液的pH,其结果如下表:
溶液 | 盐酸 | CuCl2溶液 | Na2SO4溶液 | 水 | Na2CO3溶液 | NaOH溶液 |
pH | <7 | <7 | =7 | =7 | >7 | >7 |
该同学由此得出的结论正确的是( )
A.盐溶液可能显酸性、碱性或中性
B.pH>7一定是碱溶液
C.pH=7一定是盐溶液
D.pH<7一定是酸溶液
【解答】解:A、CuCl2溶液的pH小于7,显酸性;Na2SO4溶液的pH等于7,显中性;Na2CO3溶液的pH大于7,显碱性,因此盐溶液可能显酸性、碱性或中性,故选项正确。
B、Na2CO3溶液的pH大于7,显碱性,但是碳酸钠溶液是盐溶液,故选项错误。
C、水的pH等于7,显中性,因此pH=7的溶液不一定是盐溶液,故选项错误。
D、CuCl2溶液的pH小于7,显酸性,但CuCl2溶液是盐溶液,不是酸溶液,故选项错误。
故选:A。
5.(5分)某城市水质硬度较大,容易产生水垢(细小的碳酸钙颗粒),长期使用的毛巾很容易变滑腻,你觉得可以选用厨房中的哪一种物品将水垢除去( )
A.食盐B.花生油 C.蔗糖 D.食醋
【解答】解:厨房中能用来除去水垢的物质是食醋,水垢的主要成分是碳酸钙与氢氧化镁,两者均能与醋酸反应生成可溶于水的物质。
故选:D。
6.(5分)中和反应在生活中有广泛应用.下列应用不属于中和反应的是( )
A.用盐酸除铁锈
B.服用含有氢氧化镁的药物治疗胃酸过多
C.用熟石灰改良酸性土壤
D.用硫酸处理印染厂含碱废水
【解答】解:A、用盐酸除铁锈,该反应的反应物是金属氧化物和酸,不是酸与碱生成盐和水的反应,不属于中和反应,故选项正确。
B、服用含有氢氧化镁的药物治疗胃酸过多,氢氧化镁与盐酸反应生成氯化镁和水,该反应是酸与碱反应生成盐和水的反应,属于中和反应,故选项错误。
C、用熟石灰改良酸性土壤,熟石灰与酸反应生成盐和水,该反应是酸与碱反应生成盐和水的反应,属于中和反应,故选项错误。
D、用硫酸处理印染厂含碱废水,该反应是酸与碱反应生成盐和水的反应,属于中和反应,故选项错误。
故选:A。
7.(5分)根据如图甲、乙、丙三种物质的转化关系,推测丙可能为( )
A.碳酸钙B.氧化钙 C.氢氧化钙 D.碳酸钠
【解答】解:碳酸钙在高温的条件下会分解为氧化钙和二氧化碳气体;氧化钙能与水反应生成氢氧化钙;氢氧化钙能与二氧化碳反应生成碳酸钙沉淀和水。
根据图中物质间的转化关系,丙可以与二氧化碳反应生成甲,而甲高温生成乙,乙与水反应生成丙,则推测甲、乙、丙三种物质分别为碳酸钙、氧化钙、氢氧化钙,代入检验。
故选:C。
8.(5分)25℃时,向20.0mL质量分数为30%的盐酸中滴加氢氧化钠溶液,溶液的pH与所加氢氧化钠溶液的体积如图所示,下列有关叙述正确的是( )
A.b、d点对应溶液的pH:b>d
B.所用氢氧化钠溶液的质量分数一定为30%
C.向b点对应的溶液中滴加石蕊溶液,溶液呈无色
D.d点对应的溶液中溶质是NaCl和NaOH
【解答】解:A.由图可知,b点所示溶液的pH<7;d点所示溶液的pH>7,所以b、d点对应溶液的pH:b<d,故错误;
B.由化学方程式可知:NaOH+HCl=NaCl+H2O
40 36.5
由于题干中没有提及两种溶液的密度,所以无法确定所需氢氧化钠溶液的溶质质量分数,故错误;
C.由图可知,b点所示溶液的pH<7,溶液显酸性,滴加紫色的石蕊试液变红色,故错误;
D.d点所示溶液的pH>7,所示溶液的溶质既有酸碱中和生成的氯化钠,还有过量的氢氧化钠,故正确。
故选:D。
二、我会填(共32分)
9.(12分)某校同学开展了如下“溶液酸碱性的检验”的实验活动:
(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如下表所示:
溶液 | 白醋 | 盐酸 | 蔗糖水 | 草木灰水 | 石灰水 |
加入紫薯汁 后的颜色 | 红色 | 红色 | 紫色 | 绿色 | 绿色 |
①图1中存放紫薯汁的仪器名称是 滴瓶 ;
②据上表推测,紫薯汁能做酸碱指示剂,遇到稀硫酸溶液可能显示的颜色是 红色 ;
(2)用pH试纸测定图1中部分溶液的酸碱度:草木灰水的pH>7,属于 碱性 (填“酸性”“中性”或“碱性”)溶液,白醋的pH < (填“>”“<”或“=”)7;
(3)图2是三位同学分别测定土壤酸碱度的操作示意图,其中正确的是 B (填“A”“B”或“C”,下同),可能导致被测溶液pH数值发生改变的错误操作是 C 。
【解答】解:(1)①根据实验室常用仪器可知:存放紫薯汁的仪器名称是滴瓶;
②上表推测,紫薯汁遇到稀硫酸溶液可能显示的颜色是红色,紫薯汁在酸碱溶液中显示不同颜色,可以作为酸碱指示剂;
(2)用pH试纸测定图1中部分溶液的酸碱度:草木灰水pH>7,属于碱性溶液;白醋pH<7;
(3)正确的pH试纸的使用方法是取待测液少许涂与其上进行检验,故答案为:C把pH试纸润湿会使溶液被稀释导致数值不准确,A直接放入待测液中会使溶液被污染。
故答案为:
(1)①滴瓶;②红色;
(2)碱性;<;
(3)B;C。
10.(12分)如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线。
(1)氢氧化钠和盐酸恰好完全反应时,溶液的pH 等于 7(填“大于”或“小于”或“等于”)。
(2)根据曲线判断,该反应是将 氢氧化钠溶液 (填“氢氧化钠溶液”或“盐酸”,下同)滴入 盐酸 中,理由是 在未滴入溶液之前,溶液的pH小于7,酸性溶液 。
(3)当滴入溶液的体积为5mL时,所得溶液中的溶质为 NaCl、HCl (写化学式),若在此溶液中滴入石蕊试液,溶液显 红 色。
【解答】解:(1)氢氧化钠和盐酸恰好完全反应时,氢离子和氢氧根离子均无剩余,溶液显中性,pH=7,故答案为:等于;
(2)根据图象,在反应未进行时,溶液的pH=1,为强酸性溶液,所以该曲线反应是将氢氧化钠溶液滴入盐酸中。故填:氢氧化钠溶液;盐酸;在未滴入溶液之前,溶液的pH小于7,酸性溶液;
(3)盐酸和氢氧化钠的反应原理是:HCl+NaOH=NaCl+H2O,滴入氢氧化钠溶液的体积为5mL时,溶液仍为强酸性,所以是氢氧化钠只和部分盐酸反应,所得溶液中的溶质有生成的氯化钠也有剩余的盐酸,酸使石蕊显红色,故答案为:NaCl、HCl;红。
11.(8分)某同学用盐酸与氢氧化钠按照如图的方式进行中和反应实验.
(1)反应的化学方程式为 HCl+NaOH=NaCl+H2O ;
(2)向烧杯中逐滴滴入盐酸至过量,在这个过程中,能够说明盐酸与氢氧化钠发生了化学反应的实验现象是 溶液由红色变为无色 .
(3)以下证明盐酸过量的操作及实验现象的叙述正确的是 BD (填字母代号).
A.滴加石蕊溶液,搅拌后溶液变蓝
B.滴加氢氧化钠溶液,搅拌后溶液颜色不变
C.加入蒸馏水,搅拌后溶液颜色不变
D.加入金属Zn片,产生气泡.
【解答】解:(1)盐酸和氢氧化钠发生反应的方程式为:HCl+NaOH═NaCl+H2O;
(2)氢氧化钠呈碱性,能使无色酚酞试液变红,加入盐酸的过程中要不断搅拌,使盐酸与氢氧化钠充分反应,防止局部酸液过量,酚酞在中性或酸性溶液中都显无色,当红色消失时说明盐酸与氢氧化钠发生了反应;
(3)A、滴加石蕊,溶液变蓝,说明氢氧化钠过量,盐酸不足,故A错误;
B、若恰好完全反应,滴加氢氧化钠溶液,溶液颜色应变红,若不变色则说明盐酸过量,故B正确;
C、加蒸馏水不能起到任何作用,故C错误;
D、加入金属Zn片,锌和盐酸反应产生气泡,则说明盐酸过量,故D正确.
故答案为:(1)HCl+NaOH=NaCl+H2O;(2)溶液由红色变为无色;(3)BD.
三、我会探究(18分)
12.(18分)某化学兴趣小组的同学在做氢氧化钙与盐酸中和反应的实验时,忘记滴加指示剂,因而无法判断酸碱是否恰好完全反应.于是他们对反应后溶液中的溶质大胆提出猜想,进行了以下探究,请你和他们一起完成下列实验报告.
【提出问题】该溶液中的溶质含有哪些成分?
【查阅资料】CaCl2溶液呈中性.
【猜想与假设】猜想Ⅰ:溶液中的溶质只有 CaCl2 ;
猜想Ⅱ:溶液中的溶质有CaCl2、HCl;
猜想Ⅲ:溶液中的溶质有CaCl2、Ca(OH)2;
猜想Ⅳ:溶液中的溶质有CaCl2、Ca(OH)2、HCl.
请写出该反应的化学方程式 2HCl+Ca(OH)2═CaCl2+2H2O .经过讨论,同学们直接得出猜想 Ⅳ 是不正确的.为了验证余下的哪一种猜想是正确的,同学们又做了以下实验.
【进行实验】
实验操作 | 实验现象 | 实验结论 |
①取少量反应后的溶液于试管中,滴加酚酞溶液 | 溶液不变色 | 猜想Ⅲ不正确 |
②再另取少量反应后的溶液于另一支试管中,向里面加入适量碳酸钙 | 有气泡产生 | 猜想 Ⅰ 不正确; 猜想 Ⅱ 正确 |
有气泡生成的化学方程式为 2HCl+CaCO3═CaCl2+H2O+CO2↑ .
【拓展】还可以单独用下列哪种物质来证明上述猜想是正确的 A .
A.CuO B.AgNO3 C.NaOH
反应的化学方程式为 2HCl+CuO═CuCl2+H2O .
【解答】解:【猜想与假设】反应可能是一种物质完全反应,另一种物质有剩余:若氢氧化钙过量,则含有氢氧化钙和氯化钙;若盐酸过量,则含有盐酸和氯化钙;也可能是恰好反应:只有氯化钙;氢氧化钙和盐酸反应生成了氯化钙和水,因此反应的方程式为:Ca(OH)2+2HCl═CaCl2+2H2O;可见氢氧化钙与氯化氢不能共存,所以猜想Ⅳ肯定不正确;
【进行实验】
①因为酚酞遇碱会变红色,而结论是猜想Ⅲ不正确,即不含有氢氧化钙,故观察到的现象是溶液不变红色;
②再另取少量反应后的溶液于另一支试管中,向里面加入适量CaCO3,有气泡产生,则证明剩余溶液中含有HCl,则猜想Ⅱ成立,猜想Ⅰ不成立;
碳酸钙能与稀盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
【拓展】因为烧杯内溶液中的溶质含有HCl显酸性,能用氧化铜来检验,如观察到黑色粉末溶解,溶液变成蓝色,则证明猜想Ⅱ成立;盐酸虽然能够和硝酸银反应产生沉淀,但由于其中的氯化钙也能够和硝酸银产生相同的现象,不能选择;HCl不能和排在氢后面的铜反应;氢氧化钠虽然与HCl反应,但是没有明显现象发生,无法检验;
盐酸与氧化铜反应生成氯化铜和水;反应的化学方程式为:CuO+2HCl=CuCl2+H2O.
故答案为:【猜想与假设】CaCl2;2HCl+Ca(OH)2═CaCl2+2H2O;Ⅳ.
【进行实验】溶液不变色,Ⅰ、Ⅱ;2HCl+CaCO3═CaCl2+H2O+CO2↑.
【拓展】A;2HCl+CuO═CuCl2+H2O.
四、我会计算(10分)
13.(10分)测定抗酸药物有救成分的含量胃酸的主要成分为盐酸,胃酸太多导致胃不舒服时,可以考虑服用抗酸药物来中和胃酸.某抗酸药物的有效成分为氢氧化镁,为测定氢氧化镁的含量,小霞同学取一片该药物(规格为1g)于烧杯中,加入20g溶质质量分数为3.65%的稀盐酸,恰好完全反应(假设药物中其他成分可溶于水,但不与盐酸反应).
(1)通过已知数据能求出的量有 ABCD (填字母编号,符合题意的选项都选).
A.每片药物中氢氧化镁的含量 B.反应中生成氯化镁的质量
C.反应后溶液中氯化镁的质量分数 D.20g稀盐酸中水的质量
(2)计算1g该药物中含氢氧化镁的质量(要求写出计算过程).
【解答】解:(1)A、根据氯化氢的质量结合方程式求解氢氧化镁的质量,氢氧化镁的质量除以每片质量(1g),可得每片药物中氢氧化镁的含量;
B、根据氯化氢的质量结合方程式可以求解氯化镁的质量;
C、根据氯化氢的质量结合方程式可以求解氯化镁的质量,反应后溶液的质量为20g+1g=21g,氯化镁的质量除以21g,可得反应后溶液中氯化镁的质量分数;
D、根据20g溶质质量分数为3.65%的稀盐酸,可求氯化氢的质量20g×3.65%=0.73g,则水的质量为20g﹣0.73g=19.27g.
故选ABCD;
(2)设含有氢氧化镁的质量为x
Mg(OH)2+2HCl=MgCl2十2H2O
58 73
X 20g×3.65%
x﹣=0.58g
答:l g药物中含氢氧化镁0.58 g.
故答案为:(1)ABCD;
(2)0.58g.
声明:试题解析著作权属菁优网所有,未经书面同意,不得复制发布日期:2023/9/21 20:13:01;用户:朱斌;邮箱:15348212927;学号:21219361
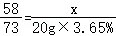
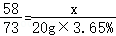
账号+密码登录
手机+密码登录
微信扫码登录
还没有账号?
立即注册